Quay lại danh sách chủ đề
Điện phân
Hóa học • Lớp 12
Cơ chế và ứng dụng của quá trình điện phân
Câu hỏi mới nhất
Hiển thị theo thứ tự cập nhật gần nhất.
Đăng nhập để lọc theo tiến độ cá nhân và xem số câu đã làm.
Xem chi tiết →
Điện phân là một ứng dụng quan trọng của dòng điện trong việc biến đổi điện năng và hóa năng. Điện phân dung dịch NaCl có màng ngăn là phương pháp chủ đạo để sản xuất các hóa chất cơ bản như NaOH và Cl\(_2\). Cho các phát biểu sau về quá trình điện phân dung dịch NaCl có màng ngăn, sử dụng các điện cực trơ:
(a) Tại cực dương (anode), xảy ra quá trình khử ion chloride thành khí chlorine.
(b) Tại cực âm (cathode), xảy ra quá trình oxi hóa nước tạo thành khí hydrogen và ion OH\(^-\).
(c) Dung dịch thu được trong quá trình điện phân có khả năng làm quỳ tím chuyển sang màu đỏ.
(d) Màng ngăn xốp có tác dụng ngăn không cho khí Cl\(_2\) tiếp xúc và phản ứng với dung dịch NaOH.
Số phát biểu đúng là
(a) Tại cực dương (anode), xảy ra quá trình khử ion chloride thành khí chlorine.
(b) Tại cực âm (cathode), xảy ra quá trình oxi hóa nước tạo thành khí hydrogen và ion OH\(^-\).
(c) Dung dịch thu được trong quá trình điện phân có khả năng làm quỳ tím chuyển sang màu đỏ.
(d) Màng ngăn xốp có tác dụng ngăn không cho khí Cl\(_2\) tiếp xúc và phản ứng với dung dịch NaOH.
Số phát biểu đúng là
Xem chi tiết →
Điện phân dung dịch CuSO₄, nhóm học sinh tiến hành thí nghiệm như sau: Nhúng hai điện cực vào cốc chứa khoảng 60 mL dung dịch CuSO₄ 0,5 M, sau đó nối hai điện cực với nguồn điện để tiến hành điện phân (lưu ý: không để hai điện cực đã nối nguồn điện chạm vào nhau). Quá trình điện phân được thực hiện trong thời gian 5 phút với cường độ dòng điện 10 A. Sau khi quan sát hiện tượng xảy ra, một học sinh nhận xét như sau:
Xem chi tiết →
Pin điện hóa có thể kí hiệu đơn giản: kim loại (anode) - kim loại (cathode). Phản ứng oxi hóa – khử xảy ra trong một pin điện hóa là: \( X(s) + Y^{2+}(aq) \rightarrow Y(s) + X^{2+}(aq) \). Kí hiệu của pin điện hóa này là
Xem chi tiết →
Một nhóm học sinh tiến hành thí nghiệm điện phân điều chế chlorine và so sánh tính oxy hóa của chlorine với iodine như sau: Cho vào bình điện phân (có màng ngăn xốp) 300 mL dung dịch hỗn hợp NaCl 2M, KI 2M và vài giọt dung dịch hồ tinh bột, nối bình điện phân với nguồn điện một chiều (như hình vẽ bên).
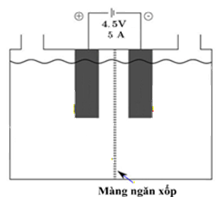
Nhóm học sinh trên tiến hành điện phân trong thời gian 30 phút với cường độ không đổi là 5 A thấy phần dung dịch bên phía anode chuyển sang màu xanh. Biết số mol electron đi qua dây dẫn được tính bằng công thức: $n = \frac{I.t}{96500}$, trong đó: $I$ là cường độ dòng điện (A), $t$ là thời gian (giây).
Sau khi tra cứu được các giá trị thế điện cực chuẩn $E^\circ_{\ce{Cl2/2Cl-}} = 1,36$ V; $E^\circ_{\ce{I2/2I-}} = 0,54$ V, nhóm học sinh đưa ra nhận định “Trong quá trình điện phân trên, ở anode chỉ có ion Cl$^-$ bị oxi hóa thành Cl$_2$, Cl$_2$ phản ứng với dung dịch KI tạo ra I$_2$ làm xanh hồ tinh bột”.

Nhóm học sinh trên tiến hành điện phân trong thời gian 30 phút với cường độ không đổi là 5 A thấy phần dung dịch bên phía anode chuyển sang màu xanh. Biết số mol electron đi qua dây dẫn được tính bằng công thức: $n = \frac{I.t}{96500}$, trong đó: $I$ là cường độ dòng điện (A), $t$ là thời gian (giây).
Sau khi tra cứu được các giá trị thế điện cực chuẩn $E^\circ_{\ce{Cl2/2Cl-}} = 1,36$ V; $E^\circ_{\ce{I2/2I-}} = 0,54$ V, nhóm học sinh đưa ra nhận định “Trong quá trình điện phân trên, ở anode chỉ có ion Cl$^-$ bị oxi hóa thành Cl$_2$, Cl$_2$ phản ứng với dung dịch KI tạo ra I$_2$ làm xanh hồ tinh bột”.
Xem chi tiết →
Khi điện phân dung dịch CuSO₄ bằng dòng điện một chiều với điện cực anode bằng Cu thì ở anode xảy ra quá trình