Môn thi
Hóa học
Thời gian
50 phút
Số câu
16
Kỳ thi
Chưa đặt nhãn
Xem trước câu hỏi
Câu 1Thông hiểu
Xem chi tiết →Cho phương trình hóa học của phản ứng: CO(g) + H2O(g) -> CO2(g) + H2(g). Viết biểu thức tốc độ của phản ứng trên. Khi nồng độ CO tăng 2 lần, nồng độ hơi nước không thay đổi, tốc độ phản ứng thay đổi như thế nào?
...
Câu 2Thông hiểu
Xem chi tiết →Cho phương trình hóa học của phản ứng: 2CO(g) + O2(g) -> 2CO2(g). Với biểu thức tốc độ tức thời là: v = k.[CO]^2.[O2], khi nồng độ mol của CO là 1 M và O2 là 1 M, hãy tính giá trị v theo k và nêu ý nghĩa của hằng số tốc độ phản ứng k.
...
Câu 3Thông hiểu
Xem chi tiết →Cho phản ứng hóa học sau: H2O2 -> H2O + 1/2O2. Biết rằng tốc độ của phản ứng này tuân theo biểu thức định luật tác dụng khối lượng. Biểu thức tốc độ phản ứng là:
A
v = k[H2O2]
B
v = k[H2O2]^2
C
v = k[H2O][O2]^1/2
D
v = k
Câu 4Thông hiểu
Xem chi tiết →Cho phản ứng hóa học sau:
2H2O2(aq) -> 2H2O(l) + O2(g)

Biết rằng tốc độ của phản ứng này tuân theo biểu thức định luật tác dụng khối lượng. Tốc độ phản ứng tức thời thay đổi như thế nào theo thời gian?
2H2O2(aq) -> 2H2O(l) + O2(g)

Biết rằng tốc độ của phản ứng này tuân theo biểu thức định luật tác dụng khối lượng. Tốc độ phản ứng tức thời thay đổi như thế nào theo thời gian?
A
Tăng dần theo thời gian.
B
Giảm dần theo thời gian.
C
Không thay đổi theo thời gian.
D
Tăng rồi giảm theo thời gian.
Câu 5Thông hiểu
Xem chi tiết →Phosgen (COCl2) là một chất độc hóa học được sử dụng trong chiến tranh thế giới thứ nhất. Phản ứng tổng hợp phosgen như sau: CO + Cl2 -> COCl2. Biểu thức tốc độ phản ứng có dạng: v = k[CO][Cl2]. Tốc độ phản ứng thay đổi như thế nào nếu tăng nồng độ CO lên 2 lần?
...
Câu 6
Xem chi tiết →Phosgen (COCl2) là một chất độc hóa học được sử dụng trong chiến tranh thế giới thứ nhất. Phản ứng tổng hợp phosgen như sau: CO + Cl2

COCl2
Biểu thức tốc độ phản ứng có dạng:
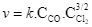
Tốc độ phản ứng thay đổi như nào nếu:
Giảm nồng độ Cl2 xuống 4 lần.

COCl2
Biểu thức tốc độ phản ứng có dạng:
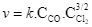
Tốc độ phản ứng thay đổi như nào nếu:
Giảm nồng độ Cl2 xuống 4 lần.
Nhập đáp án:
...
Câu 7Thông hiểu
Xem chi tiết →Ở 225 ℃, khí NO và O2 có phản ứng sau: 2NO(g) + O2(g) -> 2NO2(g). Biểu thức tốc độ phản ứng có dạng: v = k.[NO]^2.[O2]. Cho biết tốc độ phản ứng sẽ thay đổi như thế nào nếu tăng nồng độ NO lên 2 lần?
...
Câu 8Thông hiểu
Xem chi tiết →Ở 225 ℃, phản ứng giữa khí NO và O2 xảy ra như sau: 2NO(g) + O2(g) -> 2NO2(g). Biểu thức tốc độ phản ứng có dạng: v = k.[NO]^2.[O2]. Cho biết tốc độ phản ứng sẽ thay đổi như thế nào nếu giảm nồng độ O2 đi 3 lần?
...
Câu 9Thông hiểu
Xem chi tiết →Ở 225 ℃, khí NO và O2 có phản ứng sau: 2NO(g) + O2(g) -> 2NO2(g). Biểu thức tốc độ phản ứng có dạng: v = k[NO]^2[O2]. Cho biết tốc độ phản ứng sẽ thay đổi như thế nào nếu tăng nồng độ NO lên 2 lần?
...
Câu 10Thông hiểu
Xem chi tiết →Cho phản ứng đơn giản xảy ra trong bình kín: 2NO(g) + O2(g) -> 2NO2(g). Viết biểu thức tốc độ tức thời của phản ứng.
Nhập đáp án:
...
Hiển thị 10 trên 16 câu hỏi