Môn thi
Hóa học
Thời gian
50 phút
Số câu
10
Kỳ thi
Chưa đặt nhãn
Xem trước câu hỏi
Câu 1Thông hiểu
Xem chi tiết →Từ phổ khối lượng (MS) của magnesium (Mg) ở hình dưới đây:
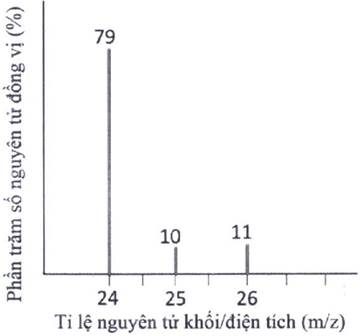
Hãy cho biết giá trị nguyên tử khối trung bình của magnesium là bao nhiêu? (Làm tròn kết quả đến hàng phần mười)

Hãy cho biết giá trị nguyên tử khối trung bình của magnesium là bao nhiêu? (Làm tròn kết quả đến hàng phần mười)
Nhập đáp án:
...
Câu 2
Xem chi tiết →Phổ khối, hay phổ khối lượng chủ yếu được sử dụng để xác định phân tử khối, nguyên tử khối của các chất và hàm lượng các đồng vị bền của một nguyên tố. Trong phổ khối lượng của mẫu chất chứa chlorine (Cl) sẽ xuất biện hai tín hiệu có giá trị m/z bằng 35 và 37 ứng với 35Cl và 37Cl có cường độ tương ứng với tỉ lệ xấp xỉ là 3: 1. Do vậy, đồng vị 35Cl chiếm khoảng 75,76% và đồng vị 37Cl chiếm khoảng 24,24% về số nguyên tử trong tự nhiên. Tính nguyên tử khối trung bình của chlorine.
Nhập đáp án:
...
Câu 3Thông hiểu
Xem chi tiết →Phổ khối, hay phổ khối lượng chủ yếu được sử dụng để xác định phân tử khối, nguyên tử khối của các chất và hàm lượng các đồng vị bền của một nguyên tố. Phổ khối của neon được biểu diễn như hình dưới. Trục tung biểu thị hàm lượng phần trăm về số nguyên tử của từng đồng vị, trục hoành biểu thị tỉ số của nguyên tử khối (m) của mỗi đồng vị với điện tích của các ion đồng vị tương ứng (điện tích Z của các ion đồng vị neon đều bằng +1).
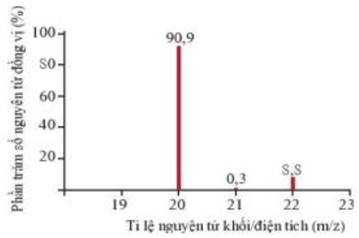
a) Neon có bao nhiêu đồng vị bền?
b) Tính nguyên tử khối trung bình của neon.

a) Neon có bao nhiêu đồng vị bền?
b) Tính nguyên tử khối trung bình của neon.
...
Câu 4Thông hiểu
Xem chi tiết →Số đồng vị bền của nguyên tố neon (Ne) được suy ra từ phổ khối lượng ở hình dưới là


A
1.
B
2.
C
3.
D
4.
Câu 5Vận dụng
Xem chi tiết →Phổ khối lượng của zirconium được biểu diễn như hình sau đây (điện tích z của các ion đồng vị zirconium đều bằng 1+).
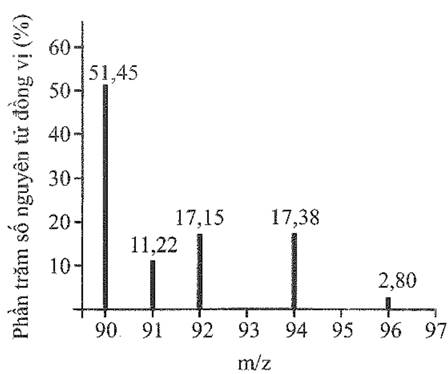
Số lượng đồng vị bền và nguyên tử khối trung bình của zirconium là:

Số lượng đồng vị bền và nguyên tử khối trung bình của zirconium là:
A
5 đồng vị, nguyên tử khối trung bình bằng 92,60.
B
5 đồng vị, nguyên tử khối trung bình bằng 91,32.
C
4 đồng vị, nguyên tử khối trung bình bằng 91,18.
D
4 đồng vị, nguyên tử khối trung bình bằng 92,00.
Câu 6Thông hiểu
Xem chi tiết →Bằng phương pháp phổ khối lượng, người ta xác định được trong tự nhiên, nguyên tố chlorine có hai đồng vị bền là 35Cl và 37Cl. Phổ khối lượng của chlorine như hình dưới đây:
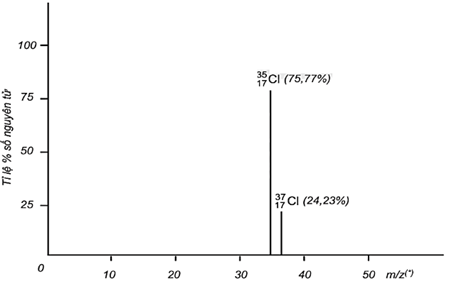
Tính nguyên tử khối trung bình của chlorine.

Tính nguyên tử khối trung bình của chlorine.
Nhập đáp án:
...
Câu 7Thông hiểu
Xem chi tiết →Cho phổ khối lượng MS của silver (Ag) ở hình dưới đây:
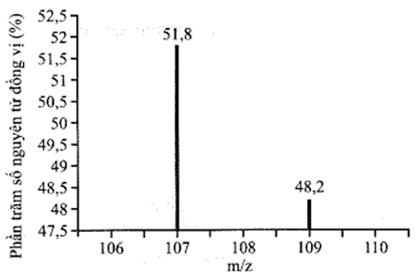
Nguyên tử khối trung bình của nguyên tố silver là

Nguyên tử khối trung bình của nguyên tố silver là
A
107,964
B
108,000
C
107,987
D
108,012
Câu 8Vận dụng
Xem chi tiết →Krypton là một trong những khí hiếm được ứng dụng trong chiếu sáng và nhiếp ảnh. Ánh sáng của krypton có nhiều dải phổ, do đó nó được sử dụng nhiều làm tia laser có mức năng lượng cao. Quan sát biểu thị phổ khối của krypton như hình dưới:
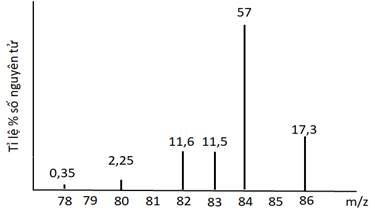
Tính thể tích của 1 gam krypton (đkc).

Tính thể tích của 1 gam krypton (đkc).
A
0,267 lít
B
0,224 lít
C
0,296 lít
D
0,448 lít
Câu 9Vận dụng
Xem chi tiết →Năm 1618, một nông dân tại Epsom nước Anh đã cho đàn bò của mình uống nước, nhưng chúng không chịu uống vì nước có vị rất đắng chát. Sau này, người ta phát hiện ra trong nước chứa magnesium sulfate (MgSO4). Bằng phương pháp phổ khối lượng, người ta xác định được magnesium có 3 đồng vị bền là 24Mg, 25Mg và 26Mg với tỉ lệ phần trăm số nguyên tử lần lượt là 79%, 10% và 11%.
a) Hãy tính nguyên tử khối trung bình của Mg.
b) Tính phần trăm khối lượng của đồng vị 24Mg có trong hợp chất MgSO4. (Cho nguyên tử khối của S = 32,065; O = 15,999; Mg = 24,32). Làm tròn kết quả đến 3 chữ số thập phân.
a) Hãy tính nguyên tử khối trung bình của Mg.
b) Tính phần trăm khối lượng của đồng vị 24Mg có trong hợp chất MgSO4. (Cho nguyên tử khối của S = 32,065; O = 15,999; Mg = 24,32). Làm tròn kết quả đến 3 chữ số thập phân.
...
Câu 10Vận dụng
Xem chi tiết →Copper(II) sulfate là một trong những thành phần chính được dùng trong thuốc trừ sâu để tạo ra kháng sinh cho cây trồng. Phổ khối của copper được biểu diễn như ở hình dưới đây:
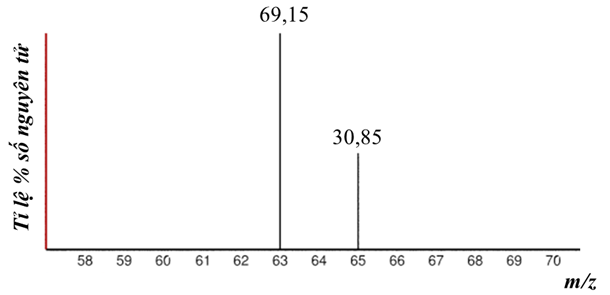
Tính thành phần phần trăm theo khối lượng của đồng vị 63Cu trong hợp chất CuSO4. (Biết nguyên tử khối trung bình của Cu là 63,546; S là 32,06; O là 16,00. Tỉ lệ phần trăm số nguyên tử của 63Cu là 69,15%)

Tính thành phần phần trăm theo khối lượng của đồng vị 63Cu trong hợp chất CuSO4. (Biết nguyên tử khối trung bình của Cu là 63,546; S là 32,06; O là 16,00. Tỉ lệ phần trăm số nguyên tử của 63Cu là 69,15%)
A
27,29%
B
69,15%
C
30,85%
D
43,75%
Hiển thị 10 trên 10 câu hỏi