Môn thi
Hóa học
Thời gian
50 phút
Số câu
15
Kỳ thi
Chưa đặt nhãn
Xem trước câu hỏi
Câu 1Thông hiểu
Xem chi tiết →Liên kết cộng hóa trị được hình thành từ cặp electron dùng chung. Để tạo nên một cặp electron chung,
A
hai AO chứa electron độc thân (hoặc giữa 1 AO trống và 1 AO bão hòa electron) cần xen phủ với nhau.
B
hai AO chứa electron bão hòa (hoặc giữa 1 AO trống và 1 AO bão hòa electron) cần xen phủ với nhau.
C
hai AO s chứa electron bão hòa cần xen phủ với nhau.
D
hai AO p chứa electron bão hòa cần xen phủ với nhau.
Câu 2Thông hiểu
Xem chi tiết →Liên kết sigma (s) là loại liên kết cộng hóa trị được hình thành do
A
sự xen phủ bên của hai orbital, vùng xen phủ nằm hai bên đường nối tâm hai nguyên tử.
B
sự xen phủ bên của hai orbital, vùng xen phủ trục nằm trên đường nối tâm hai nguyên tử.
C
sự xen phủ trục của hai orbital, vùng xen phủ nằm hai bên đường nối tâm hai nguyên tử.
D
sự xen phủ trục của hai orbital, vùng xen phủ trục nằm trên đường nối tâm hai nguyên tử.
Câu 3Thông hiểu
Xem chi tiết →Nhận xét nào sau đây không đúng khi nói về liên kết pi (p)?
A
Liên kết pi (p) là liên kết ion.
B
Liên kết pi (p) được hình thành do sự xen phủ bên của hai orbital.
C
Vùng xen phủ của hai orbital nằm hai bên đường nối tâm hai nguyên tử.
D
Liên kết pi (p) kém bền hơn liên kết sigma (s).
Câu 4Thông hiểu
Xem chi tiết →Các liên kết cộng hóa trị đơn thường là loại liên kết nào?
A
liên kết sigma (σ).
B
liên kết pi (π).
C
liên kết ion.
D
liên kết hydrogen.
Câu 5Thông hiểu
Xem chi tiết →Liên kết đôi gồm
A
hai liên kết sigma.
B
hai liên kết pi.
C
một liên kết sigma và hai liên kết pi.
D
một liên kết sigma và một liên kết pi.
Câu 6Thông hiểu
Xem chi tiết →Phân tử nào dưới đây có chứa liên kết ba?
A
Cl2
B
HCl
C
O2
D
N2
Câu 7Thông hiểu
Xem chi tiết →Sự xen phủ có sự tham gia của orbital nào luôn là xen phủ trục?
A
Orbital s.
B
Orbital p.
C
Orbital d.
D
Orbital f.
Câu 8Thông hiểu
Xem chi tiết →Vùng xen phủ giữa các orbital càng lớn thì
A
liên kết càng bền.
B
liên kết càng kém bền.
C
liên kết tạo thành thường là liên kết s.
D
liên kết tạo thành thường là liên kết p.
Câu 9Thông hiểu
Xem chi tiết →Khi hình thành phân tử giữa hai nguyên tử, vị trí của các AO như sau:
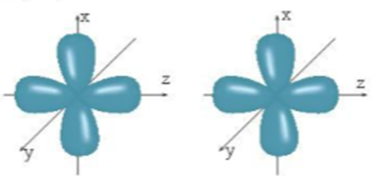
Sự xen phủ giữa hai orbital p trong trường hợp nào sẽ tạo thành liên kết s? Trong trường hợp nào sẽ tạo thành liên kết p?

Sự xen phủ giữa hai orbital p trong trường hợp nào sẽ tạo thành liên kết s? Trong trường hợp nào sẽ tạo thành liên kết p?
A
Hai AO pz xen phủ với nhau tạo liên kết p; hai AO px hoặc hai AO py xen phủ với nhau tạo liên kết s.
B
Hai AO pz xen phủ với nhau tạo liên kết s; hai AO px hoặc hai AO py xen phủ với nhau tạo liên kết p.
C
Hai AO px xen phủ với nhau tạo liên kết s; hai AO py hoặc hai AO pz xen phủ với nhau tạo liên kết p.
D
Hai AO px xen phủ với nhau tạo liên kết p; hai AO py hoặc hai AO pz xen phủ với nhau tạo liên kết s.
Câu 10Thông hiểu
Xem chi tiết →Liên kết trong phân tử H2 tạo ra là do
A
sự xen phủ của AO 2s và AO 2p.
B
sự xen phủ của AO 1s và AO 2p.
C
sự xen phủ giữa hai AO p (trục z).
D
sự xen phủ giữa hai AO 1s.
Hiển thị 10 trên 15 câu hỏi