Môn thi
Hóa học
Thời gian
50 phút
Số câu
20
Kỳ thi
Chưa đặt nhãn
Xem trước câu hỏi
Câu 1Vận dụng
Xem chi tiết →Methane là thành phần chính của khí thiên nhiên. Xét phản ứng đốt cháy methane:
CH4(g) + 2O2(g) -> CO2(g) + 2H2O(l)
Biết biến thiên enthalpy chuẩn của phản ứng là ΔrH°298 = –890,3 kJ. Nhiệt tạo thành chuẩn của CO2(g) và H2O(l) tương ứng là –393,5 kJ/mol và –285,8 kJ/mol. Hãy tính nhiệt tạo thành chuẩn của khí methane (ΔfH°298(CH4)).
CH4(g) + 2O2(g) -> CO2(g) + 2H2O(l)
Biết biến thiên enthalpy chuẩn của phản ứng là ΔrH°298 = –890,3 kJ. Nhiệt tạo thành chuẩn của CO2(g) và H2O(l) tương ứng là –393,5 kJ/mol và –285,8 kJ/mol. Hãy tính nhiệt tạo thành chuẩn của khí methane (ΔfH°298(CH4)).
...
Câu 2Vận dụng
Xem chi tiết →Cho các phản ứng sau:
(1) CaCO3(s) -> CaO(s) + CO2(g)
(2) C(graphite) + O2(g) -> CO2(g)
Tính biến thiên enthalpy chuẩn của các phản ứng trên. Biết nhiệt tạo thành chuẩn (kJ/mol) của CaCO3(s), CaO(s) và CO2(g) lần lượt là –1207, –635 và –393,5.
(1) CaCO3(s) -> CaO(s) + CO2(g)
(2) C(graphite) + O2(g) -> CO2(g)
Tính biến thiên enthalpy chuẩn của các phản ứng trên. Biết nhiệt tạo thành chuẩn (kJ/mol) của CaCO3(s), CaO(s) và CO2(g) lần lượt là –1207, –635 và –393,5.
...
Câu 3
Xem chi tiết →Quá trình hòa tan calcium chloride trong nước:
CaCl2(s)

Ca2+(aq) + 2Cl–(aq)
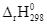
=?
Chất
CaCl2
Ca2+
Cl–
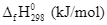
–795,0
–542,83
–167,16
Tính biến thiên enthalpy của quá trình.
CaCl2(s)

Ca2+(aq) + 2Cl–(aq)
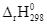
=?
Chất
CaCl2
Ca2+
Cl–
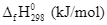
–795,0
–542,83
–167,16
Tính biến thiên enthalpy của quá trình.
Nhập đáp án:
...
Câu 4Vận dụng
Xem chi tiết →Từ số liệu bảng phụ lục, hãy xác định biến thiên enthalpy chuẩn của phản ứng đốt cháy ethane:
C2H6(g) + 7/2O2(g) -> 2CO2(g) + 3H2O(l)

C2H6(g) + 7/2O2(g) -> 2CO2(g) + 3H2O(l)

...
Câu 5
Xem chi tiết →Cho phương trình hóa học của phản ứng: C2H4(g) + H2O(l)

C2H5OH(l)
Tính biến thiên enthalpy của phản ứng theo nhiệt tạo thành chuẩn của các chất (Số liệu bảng phụ lục 2).

C2H5OH(l)
Tính biến thiên enthalpy của phản ứng theo nhiệt tạo thành chuẩn của các chất (Số liệu bảng phụ lục 2).
Nhập đáp án:
...
Câu 6Vận dụng
Xem chi tiết →Tiến hành ozone hóa 100 gam oxygen theo phản ứng sau:
3O2(g)

2O3(g)
Hỗn hợp thu được có chứa 24% ozone về khối lượng, tiêu tốn 71,2 kJ. Nhiệt tạo thành
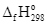
của ozone (kJ/mol) có giá trị là
3O2(g)

2O3(g)
Hỗn hợp thu được có chứa 24% ozone về khối lượng, tiêu tốn 71,2 kJ. Nhiệt tạo thành
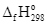
của ozone (kJ/mol) có giá trị là
A
142,4.
B
284,8.
C
–142,4.
D
–284,8.
Câu 7Vận dụng
Xem chi tiết →Cho biến thiên enthalpy của phản ứng sau ở điều kiện chuẩn: CO(g) + 1/2O2(g) -> CO2(g) có ΔrH°298 = –283,0 kJ. Biết nhiệt tạo thành chuẩn của CO2 là ΔfH°298(CO2(g)) = –393,5 kJ/mol. Nhiệt tạo thành chuẩn của CO là:
A
–110,5 kJ/mol.
B
+110,5 kJ/mol.
C
–141,5 kJ/mol.
D
–221,0 kJ/mol.
Câu 8Vận dụng
Xem chi tiết →Thành phần chính của đa số các loại đá dùng trong xây dựng là CaCO3, chúng vừa có tác dụng chịu nhiệt, vừa chịu được lực. Dựa vào bảng phụ lục 2, tính biến thiên enthalpy chuẩn (ΔrH°298) của phản ứng:
CaCO3(s) → CaO(s) + CO2(g)
Phản ứng có xảy ra thuận lợi ở điều kiện thường hay không?
CaCO3(s) → CaO(s) + CO2(g)
Phản ứng có xảy ra thuận lợi ở điều kiện thường hay không?
...
Câu 9Vận dụng
Xem chi tiết →Dựa vào enthalpy tạo thành chuẩn (ΔfH°298) của các chất: Al(s) = 0 kJ/mol; Fe2O3(s) = -824,2 kJ/mol; Fe(s) = 0 kJ/mol; Al2O3(s) = -1675,7 kJ/mol. Hãy tính biến thiên enthalpy chuẩn của phản ứng nhiệt nhôm sau: 2Al(s) + Fe2O3(s) -> 2Fe(s) + Al2O3(s). Từ kết quả tính được, hãy rút ra ý nghĩa của dấu và giá trị ΔrH°298 đối với phản ứng.
...
Câu 10
Xem chi tiết →Tính nhiệt tỏa ra khi đốt cháy hoàn toàn 12 kg khí methane (CH4), biết nhiệt tạo thành của các chất như sau:
Chất
CH4(g)
CO2(g)
H2O(l)
∆fH (kJ/mol)
–75
–392
–286
Chất
CH4(g)
CO2(g)
H2O(l)
∆fH (kJ/mol)
–75
–392
–286
Nhập đáp án:
...
Hiển thị 10 trên 20 câu hỏi