Môn thi
Hóa học
Thời gian
50 phút
Số câu
20
Kỳ thi
THPT QG
Xem trước câu hỏi
Câu 1Thông hiểu
Xem chi tiết →Nitrogen (N) thuộc nhóm VA trong bảng tuần hoàn các nguyên tố hóa học. Công thức của nitric acid (hydroxide tương ứng với oxide cao nhất của N) là
A
NO
B
HNO2
C
N2O5
D
HNO3
Câu 2Nhận biết
Xem chi tiết →Cấu hình electron của nguyên tử sắt là
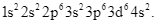
Vị trí của sắt trong bảng tuần hoàn là
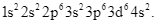
Vị trí của sắt trong bảng tuần hoàn là
A
ô số 26, chu kì 3, nhóm VIIIB.
B
ô số 26, chu kì 3, nhóm VIIIA.
C
ô số 26, chu kì 4, nhóm VIIIA.
D
ô số 26, chu kì 4, nhóm VIIIB.
Câu 3Thông hiểu
Xem chi tiết →Dãy nguyên tử nào sau đây có bán kính nguyên tử tăng dần?
A
F < S < Si < Ge < Ca < Rb.
B
Rb < Ca < Ge < Si < S < F.
C
F < Si < S < Ca < Ge < Rb.
D
F < S < Si < Ca < Ge < Rb.
Câu 4Nhận biết
Xem chi tiết →Oxide nào dưới đây tác dụng với nước tạo ra môi trường acid?
A
CaO.
B
SO3.
C
BaO.
D
Na2O.
Câu 5Thông hiểu
Xem chi tiết →Cho số hiệu nguyên tử của nguyên tố R là 7. Phát biểu nào sau đây sai?
A
Công thức oxide cao nhất của R là R2O5.
B
R có tính phi kim mạnh hơn Si (Z = 14).
C
R là nguyên tố p.
D
Nguyên tử R có 5 electron ở lớp ngoài cùng.
Câu 6Nhận biết
Xem chi tiết →Bảng tuần hoàn hiện nay không áp dụng nguyên tắc sắp xếp nào sau đây?
A
Các nguyên tố hóa học được xếp theo chiều tăng dần điện tích hạt nhân nguyên tử.
B
Các nguyên tố có cùng số lớp electron trên nguyên tử được xếp thành một hàng.
C
Các nguyên tố có cùng số electron hóa trị trong nguyên tử được xếp thành một cột.
D
Các nguyên tố được sắp xếp theo chiều tăng dần khối lượng nguyên tử.
Câu 7Nhận biết
Xem chi tiết →Magnesium là nguyên tố có khối lượng riêng nhỏ hơn một phần ba so với nhôm. Magnesium giúp cải thiện các đặc tính cơ học của nhôm khi được sử dụng làm chất tạo hợp kim. Những hợp kim này rất hữu ích trong chế tạo máy bay và ô tô. Công thức hydroxide của magnesium là
A
Mg(OH)
B
Mg(OH)2
C
MgO(OH)
D
Mg(OH)3
Câu 8Thông hiểu
Xem chi tiết →Trong một chu kì của bảng tuần hoàn các nguyên tố hóa học, theo chiều tăng dần điện tích hạt nhân, bán kính nguyên tử của các nguyên tố giảm dần do số lớp electron ... (I), lực hút giữa hạt nhân với electron lớp ngoài cùng...(II). Cụm từ cần điền vào (I), (II) lần lượt là
A
tăng dần, tăng dần.
B
giảm dần, giảm dần.
C
không đổi, tăng dần.
D
không đổi, giảm dần.
Câu 9Thông hiểu
Xem chi tiết →Phát biểu nào sau đây là đúng về xu hướng biển đổi tính kim loại trong bảng tuần hoàn các nguyên tố hoá học?
A
Tính kim loại của các nguyên tố tăng theo chiều từ trái sang phải trong một chu kì và từ trên xuống dưới trong một nhóm.
B
Tính kim loại giảm dần theo chiều từ trái sang phải trong một chu kì và tăng dần từ trên xuống dưới trong một nhóm.
C
Tính kim loại giảm dần theo chiều từ trái sang phải trong một chu kì và từ trên xuống dưới trong một nhóm.
D
Tính kim loại tăng dần theo chiều từ trái sang phải trong một chu kì và giảm dần từ trên xuống dưới trong một nhóm.
Câu 10Thông hiểu
Xem chi tiết →Biết số hiệu nguyên tử của 2 nguyên tố X và Y lần lượt là 19 và 17. Cho các phát biểu:
(a) Độ âm điện của nguyên tử X lớn hơn độ âm điện của nguyên tử Y.
(b) Số electron độc thân của nguyên tử X ít hơn số electron độc thân của nguyên tử Y.
(c) Trong các phản ứng hóa học, nguyên tử X có xu hướng nhường 1 electron.
(d) Khi hình thành liên kết với nguyên tử X, nguyên tử Y nhận 1 electron.
Số phát biểu đúng là
(a) Độ âm điện của nguyên tử X lớn hơn độ âm điện của nguyên tử Y.
(b) Số electron độc thân của nguyên tử X ít hơn số electron độc thân của nguyên tử Y.
(c) Trong các phản ứng hóa học, nguyên tử X có xu hướng nhường 1 electron.
(d) Khi hình thành liên kết với nguyên tử X, nguyên tử Y nhận 1 electron.
Số phát biểu đúng là
A
2
B
3
C
1
D
4
Hiển thị 10 trên 20 câu hỏi