Môn thi
Hóa học
Thời gian
50 phút
Số câu
20
Kỳ thi
THPT QG
Xem trước câu hỏi
Câu 1Thông hiểu
Xem chi tiết →Trong dung dịch nước, cation kim loại mạnh, gốc acid mạnh không bị thuỷ phân, còn cation kim loại trung bình và yếu bị thuỷ phân tạo môi trường acid, gốc acid yếu bị thuỷ phân tạo môi trường base. Dung dịch muối nào sau đây có

?

?
A
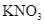
B
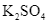
C
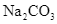
D
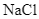
Câu 2Nhận biết
Xem chi tiết →Phát biểu nào sau đây đúng khi nói về sự điện li?
A
Sự điện li thực chất là quá trình oxi hóa – khử.
B
Sự điện li là quá trình phân li một chất dưới tác dụng của dòng điện.
C
Sự điện li là quá trình hòa tan một chất vào nước tạo thành dung dịch.
D
Sự điện li là quá trình phân li một chất trong nước thành ion.
Câu 3Thông hiểu
Xem chi tiết →Cho cân bằng sau diễn ra trong một piston ở nhiệt độ không đổi:
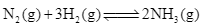
Nếu nén piston thì cân bằng sẽ chuyển dịch theo chiều nào?
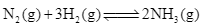
Nếu nén piston thì cân bằng sẽ chuyển dịch theo chiều nào?
A
Không thay đổi.
B
Chuyển dịch theo chiều nghịch.
C
Chuyển dịch theo chiều thuận.
D
Có thể chuyển dịch theo chiều thuận hoặc chiều nghịch tùy thuộc vào piston bị nén nhanh hay chậm.
Câu 4Thông hiểu
Xem chi tiết →Phản ứng nào sau đây, cân bằng chuyển dịch sang trái khi tăng áp suất (các điều kiện khác coi như không thay đổi)?
A
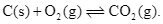
B
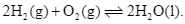
C
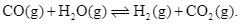
D
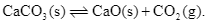
Câu 5Thông hiểu
Xem chi tiết →Tại khu vực bị ô nhiễm, pH của nước mưa đo được là 4,5 còn pH của nước mưa tại khu vực không bị ô nhiễm là 5,7. Nhận xét nào sau đây không đúng?
A
Nồng độ ion H+ trong dung dịch nước mưa bị ô nhiễm là 10^-4,5 M.
B
Nồng độ ion H+ trong dung dịch nước mưa không bị ô nhiễm là 10^-5,7 M.
C
Nồng độ ion H+ trong nước mưa bị ô nhiễm thấp hơn so với nước mưa không bị ô nhiễm.
D
Nồng độ ion H+ trong nước mưa bị ô nhiễm cao hơn so với trong nước mưa không bị ô nhiễm.
Câu 6Thông hiểu
Xem chi tiết →Cho các phát biểu sau:
(1) Khi thay đổi trạng thái cân bằng của phản ứng thuận nghịch, cân bằng sẽ chuyển dịch về phía chống lại sự thay đổi đó.
(2) Cân bằng hóa học là cân bằng tĩnh.
(3) Các yếu tố ảnh hưởng đến tốc độ phản ứng là: Nhiệt độ, nồng độ, áp suất, chất xúc tác, diện tích bề mặt.
(4) Phản ứng thuận nghịch là phản ứng xảy ra theo 2 chiều ngược nhau trong cùng điều kiện.
(5) Khi phản ứng thuận nghịch đạt trạng thái cân bằng hóa học, phản ứng dừng lại.
(6) Cân bằng hóa học là trạng thái mà phản ứng đã xảy ra hoàn toàn.
Số phát biểu đúng là
(1) Khi thay đổi trạng thái cân bằng của phản ứng thuận nghịch, cân bằng sẽ chuyển dịch về phía chống lại sự thay đổi đó.
(2) Cân bằng hóa học là cân bằng tĩnh.
(3) Các yếu tố ảnh hưởng đến tốc độ phản ứng là: Nhiệt độ, nồng độ, áp suất, chất xúc tác, diện tích bề mặt.
(4) Phản ứng thuận nghịch là phản ứng xảy ra theo 2 chiều ngược nhau trong cùng điều kiện.
(5) Khi phản ứng thuận nghịch đạt trạng thái cân bằng hóa học, phản ứng dừng lại.
(6) Cân bằng hóa học là trạng thái mà phản ứng đã xảy ra hoàn toàn.
Số phát biểu đúng là
A
4.
B
3.
C
6.
D
5.
Câu 7Thông hiểu
Xem chi tiết →Cho ba dung dịch có cùng nồng độ: hydrochloric acid (HCl), ethanoic acid (acetic acid, CH3COOH) và sodium hydroxide (NaOH). Khi chuẩn độ riêng một thể tích như nhau của dung dịch HCl và dung dịch CH3COOH bằng dung dịch NaOH, phát biểu nào sau đây là đúng?
A
Trước khi chuẩn độ, pH của hydrochloric acid lớn hơn pH của ethanoic acid.
B
Giá trị pH của hai acid tăng như nhau cho đến khi đạt điểm tương đương.
C
Cần cùng một thể tích sodium hydroxide để đạt đến điểm tương đương.
D
Tại các điểm tương đương, dung dịch của cả hai phép chuẩn độ đều có giá trị pH bằng 7.
Câu 8Thông hiểu
Xem chi tiết →Cho các chất: KOH, HBr, CH3NH2, CH3COOH, NH3. Theo thuyết Bronsted – Lowry, có bao nhiêu chất trong dãy trên là base?
A
3
B
4
C
2
D
1
Câu 9Vận dụng
Xem chi tiết → Cho cân bằng: CH4(g) + H2O(g)
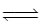
CO(g) + 3H2(g). Khi giảm nhiệt độ thì tỉ khối của hỗn hợp khí so với H2 giảm đi. Phát biểu nào sau đây là đúng?

CO(g) + 3H2(g). Khi giảm nhiệt độ thì tỉ khối của hỗn hợp khí so với H2 giảm đi. Phát biểu nào sau đây là đúng?
A
Phản ứng thuận toả nhiệt, cân bằng dịch chuyển theo chiều thuận khi tăng nhiệt độ.
B
Phản ứng thuận thu nhiệt, cân bằng dịch chuyển theo chiều thuận khi giảm nhiệt độ.
C
Phản ứng thuận thu nhiệt, cân bằng dịch chuyển theo chiều thuận khi tăng nhiệt độ.
D
Phản ứng thuận toả nhiệt, cân bằng dịch chuyển theo chiều nghịch khi tăng nhiệt độ.
Câu 10Thông hiểu
Xem chi tiết → Cho phản ứng sau:
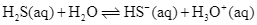
Những chất nào đóng vai trò là acid theo thuyết Bronsted – Lowry?
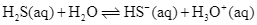
Những chất nào đóng vai trò là acid theo thuyết Bronsted – Lowry?
A
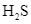 và
và 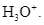
B
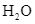 và
và 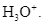
C
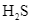 và
và 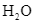
D
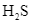 và
và 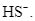
Hiển thị 10 trên 20 câu hỏi