Môn thi
Hóa học
Thời gian
50 phút
Số câu
20
Kỳ thi
THPT QG
Xem trước câu hỏi
Câu 1Thông hiểu
Xem chi tiết →Chất nào sau đây không tạo được liên kết hydrogen giữa các phân tử?
A
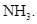
B
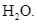
C
HF
D
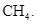
Câu 2Nhận biết
Xem chi tiết →Liên kết hóa học là
A
sự kết hợp giữa các hạt cơ bản hình thành nguyên tử bền vững.
B
sự kết hợp giữa các nguyên tử tạo thành phân tử hay tinh thể bền vững hơn.
C
sự kết hợp của các phân tử hình thành các chất bền vững.
D
sự kết hợp của chất tạo thành vật thể bền vững.
Câu 3Nhận biết
Xem chi tiết →Liên kết σ là liên kết được hình thành do
A
sự xen phủ bên của 2 orbital.
B
cặp electron chung.
C
lực hút tĩnh điện giữa hai ion.
D
sự xen phủ trục của hai orbital.
Câu 4Thông hiểu
Xem chi tiết →Khi hình thành liên kết hóa học, nguyên tử có số hiệu nguyên tử nào sau đây có xu hướng nhường 1 electron để đạt tới cấu hình electron bền vững theo quy tắc octet?
A
Z = 12
B
Z = 9
C
Z = 11
D
Z = 10
Câu 5Thông hiểu
Xem chi tiết →Cho bảng số liệu sau:
Chất
Nước (
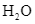
)
Hydrogen sulfide (
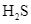
)
Nhiệt độ sôi (
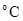
) ở 1 atm
100,0
- 60,7
Phát biểu nào sau đây sai?
Chất
Nước (
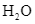
)
Hydrogen sulfide (
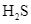
)
Nhiệt độ sôi (
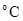
) ở 1 atm
100,0
- 60,7
Phát biểu nào sau đây sai?
A
Liên kết O – H trong phân tử H2O phân cực hơn liên kết S – H trong phân tử H2S.
B
Số liên kết trong phân tử H2O bằng số liên kết trong phân tử H2S.
C
Trong phân tử H2O và phân tử H2S chỉ có các liên kết cộng hóa trị.
D
Do có liên kết hydrogen giữa các phân tử nên nước có nhiệt độ sôi cao hơn hydrogen sulfide.
Câu 6Thông hiểu
Xem chi tiết →Dãy gồm các chất trong phân tử chỉ có liên kết cộng hoá trị phân cực là
A
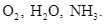
B
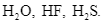
C

D
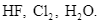
Câu 7Thông hiểu
Xem chi tiết →Trong phân tử HF, số cặp electron dùng chung và cặp electron hóa trị riêng của nguyên tử F lần lượt là
A
1 và 4.
B
1 và 3.
C
3 và 1.
D
2 và 2.
Câu 8Thông hiểu
Xem chi tiết → Nguyên tử nitrogen và nguyên tử nhôm có xu hướng nhận hay nhường lần lượt bao nhiêu electron để đạt được cấu hình bền vững?
A
Nhận 5 electron, nhường 5 electron.
B
Nhận 3 electron, nhường 3 electron.
C
Nhường 3 electron, nhận 3 electron.
D
Nhường 5 electron, nhận 5 electron.
Câu 9Nhận biết
Xem chi tiết →Trong phân tử carbon dioxide (CO2), số liên kết σ và liên kết π lần lượt là
A
4 và 0.
B
3 và 1.
C
2 và 2.
D
0 và 4.
Câu 10Thông hiểu
Xem chi tiết →Cho các hình biểu diễn sự xen phủ orbital nguyên tử để tạo liên kết hóa học sau:
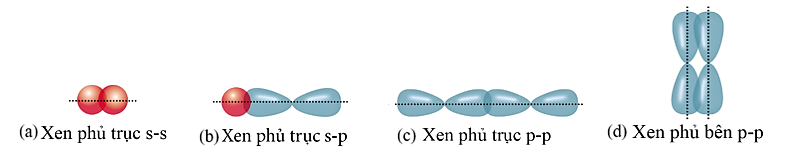
Biết số hiệu các nguyên tử của H, F và S lần lượt là 1, 9 và 16. Sự tạo thành liên kết trong các phân tử
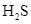
và
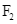
theo kiểu xen phủ tương ứng là

Biết số hiệu các nguyên tử của H, F và S lần lượt là 1, 9 và 16. Sự tạo thành liên kết trong các phân tử
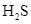
và
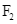
theo kiểu xen phủ tương ứng là
A
(b) và (c).
B
(a) và (c).
C
(c) và (d).
D
(b) và (d).
Hiển thị 10 trên 20 câu hỏi