Môn thi
Hóa học
Thời gian
50 phút
Số câu
20
Kỳ thi
THPT QG
Xem trước câu hỏi
Câu 1Thông hiểu
Xem chi tiết →Cho phương trình nhiệt hóa học của phản ứng:
CO2(g) -> CO(g) + 1/2 O2(g); ΔrH°298 = + 280 kJ
Lượng nhiệt cần cung cấp để tạo thành 56 g CO(g) là
CO2(g) -> CO(g) + 1/2 O2(g); ΔrH°298 = + 280 kJ
Lượng nhiệt cần cung cấp để tạo thành 56 g CO(g) là
A
140 kJ.
B
560 kJ.
C
–140 kJ.
D
–560 kJ.
Câu 2Thông hiểu
Xem chi tiết →Phản ứng nào sau đây là phản ứng toả nhiệt?
A
Phản ứng nhiệt phân muối KNO3.
B
Phản ứng phân huỷ khí NH3.
C
Phản ứng oxi hoá glucose trong cơ thể.
D
Phản ứng hoà tan 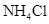 trong nước.
trong nước.
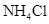 trong nước.
trong nước.Câu 3Nhận biết
Xem chi tiết →Cho hai phương trình nhiệt hóa học sau:
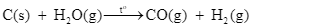
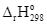
= +131,25 kJ (1)
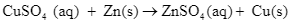
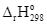
= −231,04 kJ (2)
Trong hai phản ứng trên, phản ứng nào là thu nhiệt, phản ứng nào là tỏa nhiệt?
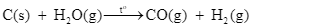
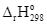
= +131,25 kJ (1)
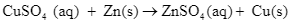
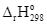
= −231,04 kJ (2)
Trong hai phản ứng trên, phản ứng nào là thu nhiệt, phản ứng nào là tỏa nhiệt?
A
Phản ứng (1) tỏa nhiệt và phản ứng (2) thu nhiệt.
B
Cả 2 phản ứng đều tỏa nhiệt.
C
Cả 2 phản ứng đều thu nhiệt.
D
Phản ứng (1) thu nhiệt và phản ứng (2) tỏa nhiệt.
Câu 4Thông hiểu
Xem chi tiết →Phương trình hóa học nào dưới đây biểu thị enthalpy tạo thành chuẩn của CO(g)?
A
2C(graphite) + O2(g) -> 2CO(g)
B
C(graphite) + 2O(g) -> CO2(g)
C
C(graphite) + 1/2O2(g) -> CO(g)
D
C(graphite) + O2(g) -> CO2(g)
Câu 5Vận dụng
Xem chi tiết →Cho enthalpy tạo thành chuẩn của một số chất như sau:
Chất
TiCl4(g)
H2O(l)
TiO2(s)
HCl(g)
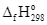
(kJ/mol)
-763
-286
-945
-92
Biến thiên enthalpy chuẩn của phản ứng
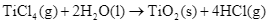
là
Chất
TiCl4(g)
H2O(l)
TiO2(s)
HCl(g)
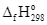
(kJ/mol)
-763
-286
-945
-92
Biến thiên enthalpy chuẩn của phản ứng
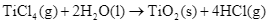
là
A
+3 kJ.
B
+22 kJ.
C
−22 kJ.
D
−3229 kJ.
Câu 6Thông hiểu
Xem chi tiết →Calcium oxide (CaO) đã phản với nước trong một cốc chịu nhiệt theo phương trình:
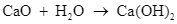
Ghi nhận giá trị nhiệt độ sau khoảng 2 phút thấy nhiệt độ chất lỏng trong cốc tăng lên từ
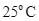
đến
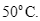
Kết luận nào sau đây là đúng?
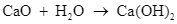
Ghi nhận giá trị nhiệt độ sau khoảng 2 phút thấy nhiệt độ chất lỏng trong cốc tăng lên từ
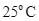
đến
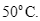
Kết luận nào sau đây là đúng?
A
Phản ứng trên là phản ứng thu nhiệt.
B
Phản ứng trên có giá trị ΔH > 0.
C
Phản ứng có năng lượng của hệ chất phản ứng nhỏ hơn năng lượng của hệ chất sản phẩm.
D
Phản ứng trên giải phóng năng lượng dưới dạng nhiệt.
Câu 7Nhận biết
Xem chi tiết →Cho các phương trình nhiệt hóa học:
(1)
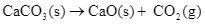
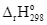
= +176,0 kJ.
(2)
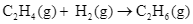
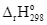
= −137,0 kJ.
(3)
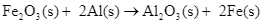
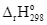
= −851,5 kJ.
Trong các phản ứng trên, phản ứng tỏa nhiệt là
(1)
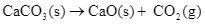
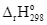
= +176,0 kJ.
(2)
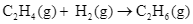
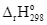
= −137,0 kJ.
(3)
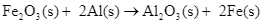
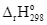
= −851,5 kJ.
Trong các phản ứng trên, phản ứng tỏa nhiệt là
A
(1), (3).
B
(2), (3).
C
(2).
D
(1).
Câu 8Nhận biết
Xem chi tiết →Công thức tính biến thiên enthalpy của phản ứng dựa vào năng lượng liên kết là
A
ΔrH298o = ΣEb(cđ) - ΣEb(sp)
B
ΔrH298o = ΣEb(sp) - ΣEb(cđ)
C
ΔrH298o = ΣEb(cđ) + ΣEb(sp)
D
ΔrH298o = ΣEb(sp) + ΣEb(cđ)
Câu 9Nhận biết
Xem chi tiết →Phát biểu nào sau đây đúng về điều kiện chuẩn?
A
Là điều kiện ứng với áp suất 1 bar (với chất khí), nồng độ 1 mol/L (đối với chất tan trong dung dịch) và nhiệt độ thường được chọn là 298 K.
B
Là điều kiện ứng với nhiệt độ 298 K và áp suất 1 atm.
C
Là điều kiện ứng với 760 mmHg.
D
Là điều kiện ứng với áp suất 1 atm và nhiệt độ 0 độ C (273 K).
Câu 10Vận dụng
Xem chi tiết →Năng lượng liên kết Cl – Cl là 243 kJ/mol, của H – H là 436 kJ/mol. Cho biết enthalpy tạo thành chuẩn của HCl là −91 kJ/mol. Năng lượng liên kết của H – Cl là:
A
430,5 kJ/mol
B
290,0 kJ/mol
C
490,0 kJ/mol
D
245,0 kJ/mol
Hiển thị 10 trên 20 câu hỏi