Môn thi
Hóa học
Thời gian
50 phút
Số câu
19
Kỳ thi
Chưa đặt nhãn
Xem trước câu hỏi
Câu 1Thông hiểu
Xem chi tiết →Phản ứng nào sau đây là phản ứng tỏa nhiệt?
A
Phản ứng nhiệt phân muối KNO3.
B
Phản ứng phân hủy khí NH3.
C
Phản ứng oxi hóa glucose trong cơ thể.
D
Phản ứng hòa tan NH4Cl trong nước.
Câu 2Nhận biết
Xem chi tiết →Phương trình nhiệt hóa học là
A
phương trình phản ứng hóa học xảy ra trong điều kiện cung cấp nhiệt độ.
B
phương trình phản ứng hóa học có kèm theo nhiệt phản ứng.
C
phương trình phản ứng hóa học có kèm theo nhiệt phản ứng và trạng thái của các chất đầu và sản phẩm.
D
phương trình phản ứng hóa học tỏa nhiệt ra môi trường.
Câu 3Thông hiểu
Xem chi tiết →Những ngày nóng nực, pha viên sủi vitamin C vào nước để giải khát, khi viên sủi tan, thấy nước trong cốc mát hơn đó là do
A
xảy ra phản ứng thu nhiệt.
B
xảy ra phản ứng tỏa nhiệt.
C
xảy ra phản ứng trao đổi chất với môi trường.
D
có sự giải phóng nhiệt lượng ra ngoài môi trường.
Câu 4Thông hiểu
Xem chi tiết →Các phản ứng tỏa nhiệt thường diễn ra
A
thuận lợi hơn các phản ứng thu nhiệt.
B
khó khăn hơn các phản ứng thu nhiệt.
C
thuận lợi hơn khi càng tỏa nhiều nhiệt.
D
thuận lợi hơn khi càng tỏa ít nhiệt.
Câu 5Thông hiểu
Xem chi tiết →Nung KNO3 lên 550 oC xảy ra phản ứng:
2KNO3(s) -> 2KNO2(s) + O2(g) (∆H > 0)
Phản ứng nhiệt phân KNO3 là
2KNO3(s) -> 2KNO2(s) + O2(g) (∆H > 0)
Phản ứng nhiệt phân KNO3 là
A
tỏa nhiệt, có ∆H < 0.
B
thu nhiệt, ∆H > 0
C
tỏa nhiệt, ∆H > 0.
D
thu nhiệt, có ∆H < 0.
Câu 6Thông hiểu
Xem chi tiết →Cho phương trình nhiệt hóa học của phản ứng:
N2(g) + O2(g) -> 2NO(g)
ΔrH°298 = +179,20 kJ
Phản ứng trên là phản ứng:
N2(g) + O2(g) -> 2NO(g)
ΔrH°298 = +179,20 kJ
Phản ứng trên là phản ứng:
A
thu nhiệt.
B
tỏa nhiệt.
C
không có sự thay đổi năng lượng.
D
có sự giải phóng nhiệt lượng ra môi trường.
Câu 7
Xem chi tiết →Dựa vào phương trình nhiệt hóa học của các phản ứng sau:
(1) CS2(l) + 3O2(g)
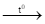
CO2(g) + 2SO2(g)
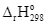
= –1110,21 kJ
(2) CO2(g)

CO(g) + 1/2O2(g)
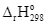
= +280,00 kJ
(3) Na(s) + 2H2O(l)

NaOH(aq) + H2(g)
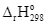
= –367,50 k
(4) ZnSO4(s)

ZnO(s) + SO3(g)
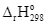
= +235,21 kJ
Cặp phản ứng thu nhiệt là
(1) CS2(l) + 3O2(g)
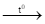
CO2(g) + 2SO2(g)
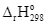
= –1110,21 kJ
(2) CO2(g)

CO(g) + 1/2O2(g)
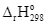
= +280,00 kJ
(3) Na(s) + 2H2O(l)

NaOH(aq) + H2(g)
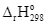
= –367,50 k
(4) ZnSO4(s)

ZnO(s) + SO3(g)
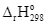
= +235,21 kJ
Cặp phản ứng thu nhiệt là
A
(1) và (2).
B
(3) và (4).
C
(1) và (3).
D
(2) và (4).
Câu 8Thông hiểu
Xem chi tiết →Enthalpy tạo thành chuẩn của một đơn chất bền
A
là biến thiên enthalpy chuẩn của phản ứng giữa nguyên tố đó với hydrogen.
B
là biến thiên enthalpy chuẩn của phản ứng giữa nguyên tố đó với oxygen.
C
được xác định từ nhiệt độ nóng chảy của nguyên tố đó.
D
bằng 0.
Câu 9Thông hiểu
Xem chi tiết →Cho phương trình nhiệt hóa học của phản ứng trung hòa sau:
HCl(aq) + NaOH(aq)

NaCl(aq) + H2O(l) ∆H = –57,3 kJ
Phát biểu nào sau đây không đúng?
HCl(aq) + NaOH(aq)

NaCl(aq) + H2O(l) ∆H = –57,3 kJ
Phát biểu nào sau đây không đúng?
A
Cho 1 mol HCl tác dụng với NaOH dư tỏa nhiệt lượng là 57,3 kJ.
B
Cho HCl dư tác dụng với 1 mol NaOH tỏa nhiệt lượng là 57,3 kJ.
C
Cho 1 mol HCl tác dụng với 1 mol NaOH tỏa nhiệt lượng là 57,3 kJ.
D
Cho 2 mol HCl tác dụng với NaOH dư tỏa nhiệt lượng là 57,3 kJ.
Câu 10Thông hiểu
Xem chi tiết →Dựa vào phương trình nhiệt hóa học của phản ứng sau: CO2(g) -> CO(g) + 1/2O2(g) có ΔrH298 = +280 kJ. Giá trị ΔrH298 của phản ứng: 2CO2(g) -> 2CO(g) + O2(g) là
A
+140 kJ.
B
–1120 kJ.
C
+560 kJ.
D
–420 kJ.
Hiển thị 10 trên 19 câu hỏi