Môn thi
Hóa học
Thời gian
50 phút
Số câu
20
Kỳ thi
THPT QG
Xem trước câu hỏi
Câu 1Thông hiểu
Xem chi tiết →Cho phương trình nhiệt hóa học của phản ứng trung hòa sau:
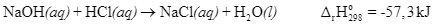
Phát biểu nào sau đây không đúng?
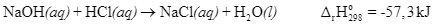
Phát biểu nào sau đây không đúng?
A
Biến thiên enthalpy chuẩn của phản ứng là -57,3 kJ.
B
Phản ứng trên là phản ứng tỏa nhiệt.
C
Nhiệt tạo thành chuẩn của NaCl (aq) là -57,3 kJ/mol.
D
Phản ứng trên giải phóng nhiệt năng ra môi trường.
Câu 2Nhận biết
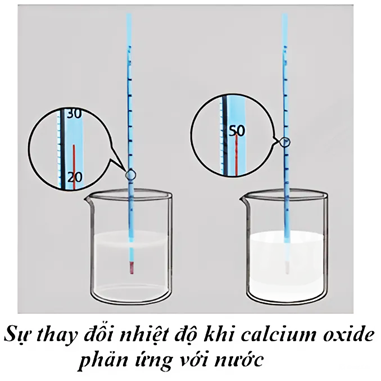
Xem chi tiết →Sự thay đổi nhiệt độ trong phản ứng của calcium với nước được minh họa trong hình bên dưới. Phản ứng của calcium với nước là

A
phản ứng thu nhiệt.
B
phản ứng phân hủy.
C
phản ứng tỏa nhiệt.
D
phản ứng thuận nghịch.
Câu 3Nhận biết
Xem chi tiết →Cho các phương trình nhiệt hóa học sau:
(1) ZnO(s) + SO3(g) -> ZnSO4(s) ; ΔrH°298 = -235,21 kJ
(2) 2Na(s) + 2H2O(l) -> 2NaOH(aq) + H2(g) ; ΔrH°298 = -367,50 kJ
(3) CO2(g) -> CO(g) + 1/2O2(g) ; ΔrH°298 = +280,00 kJ
(4) C3H8(g) + 5O2(g) -> 3CO2(g) + 4H2O(l) ; ΔrH°298 = -2219,00 kJ
Phản ứng thu nhiệt là:
(1) ZnO(s) + SO3(g) -> ZnSO4(s) ; ΔrH°298 = -235,21 kJ
(2) 2Na(s) + 2H2O(l) -> 2NaOH(aq) + H2(g) ; ΔrH°298 = -367,50 kJ
(3) CO2(g) -> CO(g) + 1/2O2(g) ; ΔrH°298 = +280,00 kJ
(4) C3H8(g) + 5O2(g) -> 3CO2(g) + 4H2O(l) ; ΔrH°298 = -2219,00 kJ
Phản ứng thu nhiệt là:
A
(1).
B
(2).
C
(4).
D
(3).
Câu 4Nhận biết
Xem chi tiết →Kí hiệu biến thiên enthalpy (nhiệt phản ứng) của phản ứng ở điều kiện chuẩn là
A
ΔrH°298
B
ΔrH
C
ΔfH°298
D
ΔcH°298
Câu 5Thông hiểu
Xem chi tiết →Cho các phát biểu:
(a) Tất cả các phản ứng cháy đều tỏa nhiệt.
(b) Phản ứng tỏa nhiệt là phản ứng giải phóng năng lượng dưới dạng nhiệt.
(c) Tất cả các phản ứng mà chất tham gia có chứa nguyên tố oxygen đều tỏa nhiệt.
(d) Phản ứng thu nhiệt là phản ứng hấp thụ năng lượng dưới dạng nhiệt.
(e) Lượng nhiệt mà phản ứng hấp thụ hay giải phóng không phụ thuộc vào điều kiện thực hiện phản ứng và thể tồn tại của chất trong phản ứng.
(g) Sự cháy của nhiên liệu (xăng, dầu, khí gas, than, gỗ,…) là những ví dụ về phản ứng thu nhiệt vì cần khơi mào.
Số phát biểu đúng là
(a) Tất cả các phản ứng cháy đều tỏa nhiệt.
(b) Phản ứng tỏa nhiệt là phản ứng giải phóng năng lượng dưới dạng nhiệt.
(c) Tất cả các phản ứng mà chất tham gia có chứa nguyên tố oxygen đều tỏa nhiệt.
(d) Phản ứng thu nhiệt là phản ứng hấp thụ năng lượng dưới dạng nhiệt.
(e) Lượng nhiệt mà phản ứng hấp thụ hay giải phóng không phụ thuộc vào điều kiện thực hiện phản ứng và thể tồn tại của chất trong phản ứng.
(g) Sự cháy của nhiên liệu (xăng, dầu, khí gas, than, gỗ,…) là những ví dụ về phản ứng thu nhiệt vì cần khơi mào.
Số phát biểu đúng là
A
2
B
3
C
4
D
5
Câu 6Thông hiểu
Xem chi tiết →Phương trình hóa học nào dưới đây là phương trình biểu thị enthalpy tạo thành chuẩn của một chất?
A
N2(g) + O2(g) -> 2NO(g)
B
Na(s) + 1/2Br2(l) -> NaBr(s)
C
N2(g) + O2(g) -> 2NO(g)
D
4Na(s) + O2(g) -> 2Na2O(s)
Câu 7Nhận biết
Xem chi tiết →Chất nào sau đây có nhiệt tạo thành chuẩn (ΔfH°298) bằng 0 (kJ/mol)?
A
NaCl(s).
B
CO2(g).
C
H2O(l).
D
H2(g).
Câu 8Nhận biết
Xem chi tiết →Công thức tính biến thiên enthalpy của phản ứng theo năng lượng liên kết (trong đó, kí hiệu
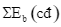
là tổng năng lượng liên kết của các chất tham gia phản ứng; kí hiệu
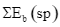
là tổng năng lượng liên kết của các chất sản phẩm phản ứng) là
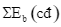
là tổng năng lượng liên kết của các chất tham gia phản ứng; kí hiệu
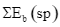
là tổng năng lượng liên kết của các chất sản phẩm phản ứng) là
A
\(\Delta_r H_{298}^o = \sum E_b(sp) - \sum E_b(cd)\)
B
\(\Delta_r H_{298}^o = \sum E_b(cd) + \sum E_b(sp)\)
C
\(\Delta_r H_{298}^o = \sum E_b(cd) - \sum E_b(sp)\)
D
\(\Delta_r H_{298}^o = \sum E_b(sp) \times \sum E_b(cd)\)
Câu 9Nhận biết
Xem chi tiết →Phản ứng thu nhiệt là phản ứng có
A
∆rH = 0
B
∆rH < 0
C
∆rH > 0
D
∆rH ≤ 0
Câu 10Nhận biết
Xem chi tiết →Phát biểu nào sau đây đúng?
A
Điều kiện chuẩn là điều kiện ứng với áp suất 1 bar (với chất khí), nồng độ 1 mol L⁻¹ (đối với chất tan trong dung dịch) và nhiệt độ thường được chọn là 298 K.
B
Điều kiện chuẩn là điều kiện ứng với nhiệt độ 298 K.
C
Áp suất 760 mmHg là áp suất ở điều kiện chuẩn.
D
Điều kiện chuẩn là điều kiện ứng với áp suất 1 atm, nhiệt độ 0 °C.
Hiển thị 10 trên 20 câu hỏi