Môn thi
Hóa học
Thời gian
50 phút
Số câu
20
Kỳ thi
THPT QG
Xem trước câu hỏi
Câu 1Thông hiểu
Xem chi tiết →PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Mỗi câu hỏi học sinh chỉ chọn một phương án.
M là nguyên tố kim loại chuyển tiếp dãy thứ nhất, có một số đặc điểm sau:
• Ở trạng thái cơ bản, nguyên tử M có 1 electron ở lớp ngoài cùng.
• Trong hợp chất, số oxi hoá phổ biến của nguyên tố M là +2.
M là nguyên tố nào sau đây?
M là nguyên tố kim loại chuyển tiếp dãy thứ nhất, có một số đặc điểm sau:
• Ở trạng thái cơ bản, nguyên tử M có 1 electron ở lớp ngoài cùng.
• Trong hợp chất, số oxi hoá phổ biến của nguyên tố M là +2.
M là nguyên tố nào sau đây?
A
Fe.
B
Ni.
C
Mn.
D
Cu.
Câu 2Thông hiểu
Xem chi tiết →Khi hoà tan hợp chất CoCl2 vào nước thì hình thành phức chất aqua có dạng hình học là bát diện. Công thức của phức chất là
A
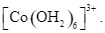
B
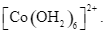
C
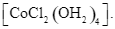
D
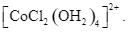
Câu 3Thông hiểu
Xem chi tiết →Trong dãy kim loại chuyển tiếp thứ nhất, hai kim loại nào sau đây đều là kim loại nhẹ (D < 5 g/cm3)?
A
Cr, Mn.
B
Sc, Ti.
C
Ni, Cu.
D
Fe, Co.
Câu 4Thông hiểu
Xem chi tiết →Phức chất có công thức [PtCl2(NH3)2] có cấu tạo như hình bên dưới:
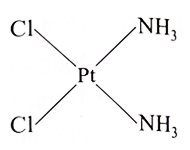
Phát biểu nào dưới đây về phức chất trên là không đúng?

Phát biểu nào dưới đây về phức chất trên là không đúng?
A
Phức chất có điện tích bằng 0.
B
Có hai loại phối tử trong phức chất.
C
Để hình thành phức chất trên thì cation 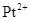 đã dùng 4 orbital trống để nhận các cặp electron hoá trị riêng của các phân tử NH3 và các anion Cl−.
đã dùng 4 orbital trống để nhận các cặp electron hoá trị riêng của các phân tử NH3 và các anion Cl−.
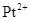 đã dùng 4 orbital trống để nhận các cặp electron hoá trị riêng của các phân tử NH3 và các anion Cl−.
đã dùng 4 orbital trống để nhận các cặp electron hoá trị riêng của các phân tử NH3 và các anion Cl−.D
Nối từng cặp phối tử cạnh nhau ở cấu tạo trên bằng một đoạn thẳng. Bốn đoạn thẳng tạo ra hình dạng của phức chất, đó là hình tứ diện.
Câu 5Thông hiểu
Xem chi tiết →Nguyên tố nào sau đây nằm trong chu kì 4 nhưng không thuộc những nguyên tố chuyển tiếp dãy thứ nhất?
A
Đồng (Cu).
B
Sắt (Fe).
C
Potassium (K).
D
Nickel (Ni).
Câu 6Nhận biết
Xem chi tiết →Nguyên tố nào sau đây được mệnh danh là “nguyên tố của màu sắc” do có khả năng thể hiện màu sắc phong phú?
A
Sắt.
B
Nickel.
C
Chromium.
D
Đồng.
Câu 7Thông hiểu
Xem chi tiết →Số hiệu nguyên tử của chromium là 24. Theo các nguyên lí và quy tắc thông thường thì cấu hình electron của nguyên tử chromium được viết ở dạng (I). Tuy nhiên, dựa vào kết quả thực nghiệm về phổ phát xạ của nguyên tử người ta cho rằng nguyên tử chromium phải có 6 electron độc thân, nên cấu hình electron của nguyên tử này được viết ở dạng (II). Dạng (I) và dạng (II) lần lượt là
A
[Ar] 3d4 4s2 và [Ar] 3d5 4s1
B
[Ar] 3d5 4s1 và [Ar] 3d4 4s2
C
[Ar] 3d3 4s2 và [Ar] 3d5 4s1
D
[Ar] 3d6 4s0 và [Ar] 3d5 4s1
Câu 8Thông hiểu
Xem chi tiết →Theo thuyết Liên kết hoá trị, tương tác giữa phối tử và nguyên tử trung tâm trong phức chất là
A
liên kết cộng hoá trị theo kiểu cho – nhận.
B
liên kết ion.
C
tương tác van der Waals.
D
liên kết hydrogen.
Câu 9Thông hiểu
Xem chi tiết →Vì sao kẽm (zinc, Z = 30) không phải là nguyên tố chuyển tiếp?
A
Vì cấu hình electron của nguyên tử Zn và cấu hình electron của ion Zn2+ đều có phân lớp 3d đã bão hoà.
B
Vì Zn không thuộc nguyên tố chu kì 4.
C
Vì Zn không phải là nguyên tố nhóm B.
D
Vì cấu hình electron của nguyên tử Zn có phân lớp d chưa bão hoà.
Câu 10Thông hiểu
Xem chi tiết →Cho các chất/ion có công thức: CuCl2, NH3,
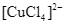
. Phát biểu nào sau đây là không đúng?
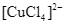
. Phát biểu nào sau đây là không đúng?
A
Do không có liên kết cộng hoá trị theo kiểu cho – nhận trong phân tử nên CuCl2 không phải là phức chất.
B
Do có nguyên tử trung tâm là nguyên tố kim loại, đồng thời các phối tử xung quanh liên kết với nguyên tử trung tâm bằng liên kết cho – nhận nên [Cu(NH3)4]2+ là phức chất.
C
Dù có các nguyên tử H xung quanh N, nhưng NH3 không phải là phức chất.
D
Do nguyên tố đồng có hoá trị II nên quanh nguyên tử Cu trong CuCl2 và trong [Cu(NH3)4]2+ đều có 2 liên kết.
Hiển thị 10 trên 20 câu hỏi