Môn thi
Hóa học
Thời gian
50 phút
Số câu
20
Kỳ thi
Chưa đặt nhãn
Xem trước câu hỏi
Câu 1Nhận biết
Xem chi tiết →Phát biểu nào sau đây đúng?
A
Điều kiện chuẩn là điều kiện ứng với áp suất 1 bar (với chất khí), nồng độ 1 mol L-1 (đối với chất tan trong dung dịch) và nhiệt độ thường được chọn là 298 K.
B
Điều kiện chuẩn là điều kiện ứng với nhiệt độ 298 K.
C
Áp suất 760 mmHg là áp suất ở điều kiện chuẩn.
D
Điều kiện chuẩn là điều kiện ứng với áp suất 1 atm, nhiệt độ 0 °C.
Câu 2Nhận biết
Xem chi tiết →Kí hiệu biến thiên enthalpy (nhiệt phản ứng) của phản ứng ở điều kiện chuẩn là
A
\(\Delta_r H^o_{298}\)
B
\(\Delta_r H\)
C
\(E_a\)
D
\(\Delta S\)
Câu 3Thông hiểu
Xem chi tiết →Chất nào sau đây có nhiệt tạo thành chuẩn (
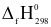
) bằng 0 (kJ/mol)?
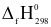
) bằng 0 (kJ/mol)?
A
NaCl(s).
B
CO2(g).
C
H2O(l).
D
H2(g).
Câu 4Thông hiểu
Xem chi tiết →Công thức tính biến thiên enthalpy của phản ứng theo năng lượng liên kết (trong đó, kí hiệu
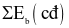
là tổng năng lượng liên kết của các chất tham gia phản ứng; kí hiệu
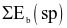
là tổng năng lượng liên kết của các chất sản phẩm phản ứng) là
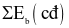
là tổng năng lượng liên kết của các chất tham gia phản ứng; kí hiệu
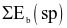
là tổng năng lượng liên kết của các chất sản phẩm phản ứng) là
A
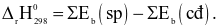
B
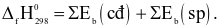
C
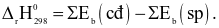
D
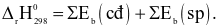
Câu 5Nhận biết
Xem chi tiết →Phản ứng thu nhiệt là phản ứng có biến thiên enthalpy chuẩn của phản ứng dương (\(\Delta_r H^0_{298} > 0\)).
A
\(\Delta_r H^0_{298} < 0\)
B
\(\Delta_r H^0_{298} = 0\)
C
\(\Delta_r H^0_{298} > 0\)
D
\(\Delta_r H^0_{298} \leq 0\)
Câu 6Thông hiểu
Xem chi tiết →Sự thay đổi nhiệt độ trong phản ứng của calcium với nước được minh họa trong hình bên dưới. Phản ứng của calcium với nước là
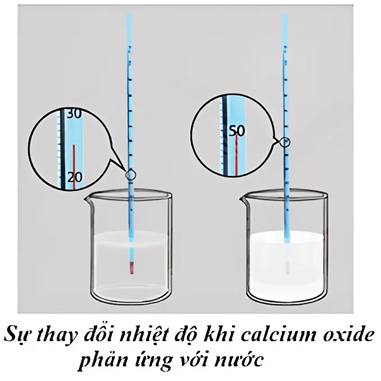

A
phản ứng thu nhiệt.
B
phản ứng phân hủy.
C
phản ứng tỏa nhiệt.
D
phản ứng thuận nghịch.
Câu 7Thông hiểu
Xem chi tiết →Khái niệm nào sau đây về enthalpy tạo thành chuẩn là chính xác nhất?
A
Là nhiệt kèm theo (thu vào hoặc tỏa ra) của phản ứng tạo thành 1 mol chất đó từ các đơn chất kém bền nhất ở điều kiện chuẩn.
B
Là nhiệt kèm theo (thu vào hoặc tỏa ra) của phản ứng tạo thành 1 mol chất đó từ các đơn chất bền nhất ở điều kiện tiêu chuẩn.
C
Là nhiệt kèm theo (thu vào hoặc tỏa ra) của phản ứng tạo thành 1 mol chất đó từ các đơn chất bền nhất ở điều kiện chuẩn.
D
Là nhiệt kèm theo (thu vào hoặc tỏa ra) của phản ứng tạo thành 2 mol chất đó từ các đơn chất bền nhất ở điều kiện chuẩn.
Câu 8Thông hiểu
Xem chi tiết →Enthalpy tạo thành chuẩn của các khí O3, CO2, NH3, HI lần lượt là 142,2
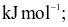
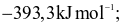
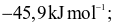
26,5
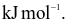
Thứ tự độ bền tăng dần của các hợp chất trên là
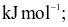
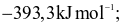
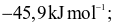
26,5
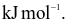
Thứ tự độ bền tăng dần của các hợp chất trên là
A
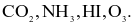
B
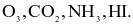
C

D
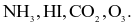
Câu 9Thông hiểu
Xem chi tiết →Cho phản ứng chuyển hóa giữa hai dạng đơn chất của carbon:
C (kim cương) → C (graphite)
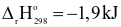
Nhận xét nào sau đây là đúng?
C (kim cương) → C (graphite)
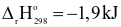
Nhận xét nào sau đây là đúng?
A
Phản ứng thu nhiệt, kim cương bền hơn graphite.
B
Phản ứng thu nhiệt, graphite bền hơn kim cương.
C
Phản ứng tỏa nhiệt, kim cương bền hơn graphite.
D
Phản ứng tỏa nhiệt, graphite bền hơn kim cương.
Câu 10Thông hiểu
Xem chi tiết →Phương trình hóa học nào sau đây biểu thị enthalpy tạo thành chuẩn của CO(g)?
A
2C(graphite) + O2(g) -> 2CO(g)
B
C(graphite) + O2(g) -> CO2(g)
C
C(graphite) + 1/2O2(g) -> CO(g)
D
CO(g) -> C(graphite) + 1/2O2(g)
Hiển thị 10 trên 20 câu hỏi