Môn thi
Hóa học
Thời gian
50 phút
Số câu
20
Kỳ thi
Chưa đặt nhãn
Xem trước câu hỏi
Câu 1Thông hiểu
Xem chi tiết →Phát biểu nào sau đây là đúng?
A
Tốc độ của phản ứng hoá học có thể có giá trị âm hoặc dương.
B
Tốc độ của phản ứng hoá học là hiệu số nồng độ của một chất trong hỗn hợp phản ứng tại hai thời điểm khác nhau.
C
Trong cùng một phản ứng hoá học, tốc độ tiêu thụ các chất phản ứng khác nhau sẽ như nhau nếu chúng được lấy với cùng một nồng độ.
D
Trong cùng một phản ứng hoá học, tốc độ tạo thành của các chất sản phẩm khác nhau là khác nhau, tuỳ thuộc vào hệ số cân bằng của chúng trong phương trình hoá học.
Câu 2Nhận biết
Xem chi tiết →Tốc độ phản ứng là
A
độ biến thiên nồng độ của một chất phản ứng trong một đơn vị thời gian.
B
độ biến thiên nồng độ của một sản phẩm phản ứng trong một đơn vị thời gian.
C
độ biến thiên nồng độ của một chất phản ứng hoặc sản phẩm phản ứng trong một đơn vị thời gian.
D
độ biến thiên nồng độ của các chất phản ứng trong một đơn vị thời gian.
Câu 3Thông hiểu
Xem chi tiết →Hằng số tốc độ phản ứng k phụ thuộc vào
A
thể tích và bản chất các chất tham gia phản ứng.
B
nhiệt độ và bản chất các chất tham gia phản ứng.
C
tốc độ độ và bản chất các chất tham gia phản ứng.
D
áp suất và bản chất các chất tham gia phản ứng.
Câu 4Thông hiểu
Xem chi tiết →Cho phản ứng đơn giản:
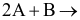
sản phẩm. Khi tăng nồng độ chất A lên gấp đôi, tốc độ phản ứng thay đổi như thế nào?
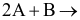
sản phẩm. Khi tăng nồng độ chất A lên gấp đôi, tốc độ phản ứng thay đổi như thế nào?
A
Tăng 2 lần.
B
Tăng 6 lần.
C
Tăng 4 lần.
D
Không đổi.
Câu 5Nhận biết
Xem chi tiết →Tốc độ tức thời của phản ứng là
A
tốc độ được tính một khoảng thời gian.
B
sự biến thiên nồng độ.
C
tốc độ được tính tại một thời điểm nhất định.
D
biến thiên khối lượng của phản ứng.
Câu 6Thông hiểu
Xem chi tiết →Trong các cặp phản ứng sau, nếu lượng Fe trong các cặp đều được lấy bằng nhau và có kích thước như nhau thì cặp nào có tốc độ phản ứng lớn nhất?
A
Fe + dung dịch HCl 0,3 M.
B
Fe + dung dịch HCl 0,5 M.
C
Fe + dung dịch HCl 0,1 M.
D
Fe + dung dịch HCl 0,2 M.
Câu 7Thông hiểu
Xem chi tiết →Cho phản ứng hóa học sau: Zn (s) + H2SO4 (aq, dư) → ZnSO4 (aq) + H2 (g)
Yếu tố nào sau đây không ảnh hưởng đến tốc độ phản ứng?
Yếu tố nào sau đây không ảnh hưởng đến tốc độ phản ứng?
A
Diện tích bề mặt Zn.
B
Nồng độ dung dịch sulfuric acid.
C
Thể tích dung dịch sulfuric acid.
D
Nhiệt độ của dung dịch sulfuric acid.
Câu 8Thông hiểu
Xem chi tiết →Củi khi được chẻ nhỏ sẽ cháy nhanh và mạnh hơn so với củi có kích thước lớn. Yếu tố nào đã được sử dụng để làm tăng tốc độ phản ứng trong trường hợp trên?
A
Chất xúc tác.
B
Diện tích bề mặt tiếp xúc.
C
Nồng độ.
D
Nhiệt độ.
Câu 9Thông hiểu
Xem chi tiết →Phản ứng nào sau đây không thay đổi tốc độ khi tăng áp suất?
A
2H2(g) + O2(g) -> 2H2O(l)
B
H2(g) + Cl2(g) -> 2HCl(g)
C
CO(g) + 2H2(g) -> CH3OH(g)
D
MgO(s) + H2SO4(aq) -> MgSO4(aq) + H2O(l)
Câu 10Thông hiểu
Xem chi tiết →Cho các biện pháp sau:
(a) Dùng khí nén, nóng thổi vào lò cao để đốt cháy than cốc (trong sản xuất gang).
(b) Bảo quản thực phẩm trong tủ lạnh để giữ thực phẩm tươi lâu.
(c) Nghiền nguyên liệu trước khi nung để sản xuất clinker.
(d) Cho bột sắt làm xúc tác trong quá trình sản xuất NH3 từ N2 và H2.
Số biện pháp được sử dụng để tăng tốc độ phản ứng là
(a) Dùng khí nén, nóng thổi vào lò cao để đốt cháy than cốc (trong sản xuất gang).
(b) Bảo quản thực phẩm trong tủ lạnh để giữ thực phẩm tươi lâu.
(c) Nghiền nguyên liệu trước khi nung để sản xuất clinker.
(d) Cho bột sắt làm xúc tác trong quá trình sản xuất NH3 từ N2 và H2.
Số biện pháp được sử dụng để tăng tốc độ phản ứng là
A
1.
B
2.
C
3.
D
4.
Hiển thị 10 trên 20 câu hỏi