Môn thi
Hóa học
Thời gian
50 phút
Số câu
20
Kỳ thi
Chưa đặt nhãn
Xem trước câu hỏi
Câu 1Thông hiểu
Xem chi tiết →Sự phân bố electron vào các lớp và phân lớp căn cứ vào
A
nguyên tử khối tăng dần.
B
số khối tăng dần.
C
mức năng lượng electron.
D
điện tích hạt nhân tăng dần.
Câu 2Nhận biết
Xem chi tiết →Kí hiệu nguyên tử nào sau đây được viết sai?
A
11^23 Na
B
13^27 Al
C
20^40 Ca
D
26^56 Fe
Câu 3Thông hiểu
Xem chi tiết →Các nguyên tử nào dưới đây thuộc cùng một nguyên tố hóa học?
A
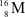 và
và 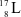
B
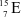 và
và 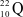
C
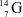 và
và 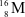
D
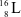 và
và 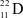
Câu 4Nhận biết
Xem chi tiết →Hạt mang điện trong nhân nguyên tử là
A
neutron.
B
proton.
C
electron.
D
proton và neutron.
Câu 5Thông hiểu
Xem chi tiết →Photpho có Z=15 tổng số electron của lớp ngoài cùng là
A
3
B
4
C
5
D
6
Câu 6Nhận biết
Xem chi tiết →Vỏ nguyên tử gồm các electron chuyển động như thế nào xung quanh hạt nhân?
A
Chuyển động rất chậm và theo những quỹ đạo xác định.
B
Chuyển động rất nhanh và theo những quỹ đạo xác định.
C
Chuyển động rất chậm và không theo những quỹ đạo xác định.
D
Chuyển động rất nhanh và không theo những quỹ đạo xác định.
Câu 7Vận dụng
Xem chi tiết →Nguyên tố chlorine (Cl) có hai đồng vị bền với tỉ lệ phần trăm số nguyên tử tương ứng là: ^{35}Cl chiếm 75,77% và ^{37}Cl chiếm 24,23%. Trong phân tử CaCl_{2}, phần trăm khối lượng của ^{35}Cl là bao nhiêu? (Cho nguyên tử khối trung bình của Cl là 35,5; Ca = 40)
A
23,9%.
B
47,8%.
C
16,2%.
D
75,8%.
Câu 8Nhận biết
Xem chi tiết →Phân lớp 3d có số electron tối đa là
A
6
B
10
C
14
D
18
Câu 9Nhận biết
Xem chi tiết →Electron thuộc lớp nào sau đây liên kết chặt chẽ nhất với hạt nhân?
A
Lớp N.
B
Lớp L.
C
Lớp M.
D
Lớp K.
Câu 10Nhận biết
Xem chi tiết →Orbital s có dạng
A
hình bầu dục.
B
hình số 8 nổi.
C
hình tròn.
D
hình cầu.
Hiển thị 10 trên 20 câu hỏi