Môn thi
Hóa học
Thời gian
50 phút
Số câu
20
Kỳ thi
THPT QG
Xem trước câu hỏi
Câu 1Thông hiểu
Xem chi tiết →Nhiệt tạo thành chuẩn \((\Delta_f H^\circ_{298})\) của \(Fe_2O_3(s)\), \(Al_2O_3(s)\) và \(Fe(s)\) lần lượt là –824,2 kJ/mol; –1675,7 kJ/mol và 0 kJ/mol. Biến thiên enthalpy chuẩn \((\Delta_r H^\circ_{298})\) của phản ứng \(Fe_2O_3(s) + 2Al(s) \rightarrow Al_2O_3(s) + 2Fe(s)\) là bao nhiêu?
A
–851,5 kJ.
B
+851,5 kJ.
C
+2499,9 kJ.
D
2499,9 kJ.
Câu 2Thông hiểu
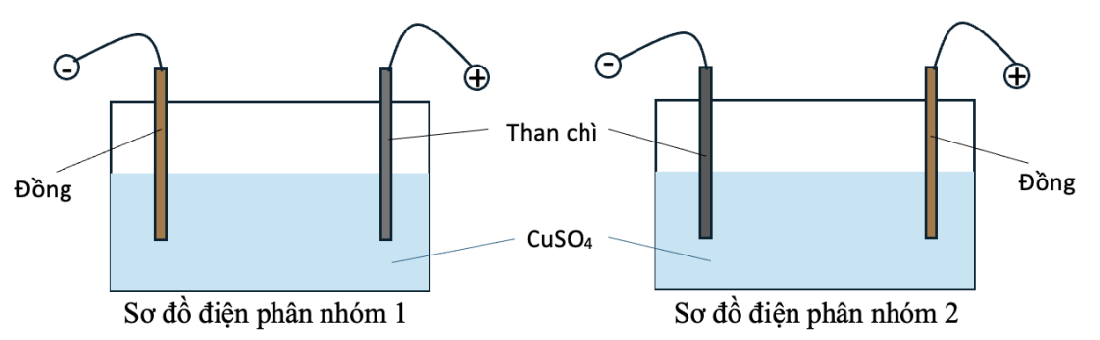
Xem chi tiết →Hai nhóm học sinh tiến hành thí nghiệm điện phân dung dịch \(CuSO_4\) với một điện cực than chì và một điện cực bằng đồng (bỏ qua sự thay đổi thể tích của dung dịch khi điện phân).
Nhóm 1: Nối điện cực than chì với cực dương và điện cực đồng với cực âm của nguồn điện.
Nhóm 2: Nối điện cực than chì với cực âm và điện cực đồng với cực dương của nguồn điện.
Phát biểu nào sau đây đúng?
Nhóm 1: Nối điện cực than chì với cực dương và điện cực đồng với cực âm của nguồn điện.
Nhóm 2: Nối điện cực than chì với cực âm và điện cực đồng với cực dương của nguồn điện.

Phát biểu nào sau đây đúng?
A
Ở nhóm 1, pH của dung dịch điện phân tăng dần.
B
Ở nhóm 1, nồng độ \(Cu^{2+}\)) trong dung dịch không thay đổi.
C
Đối với cả hai nhóm đều có kim loại đồng bám vào anode.
D
Ở nhóm 2, tại anode xảy ra quá trình oxi hóa đồng.
Câu 3Thông hiểu
Xem chi tiết →Cho các dung dịch có cùng nồng độ mol: Na₂CO₃, H₂SO₄, HCl, KNO₃. Dung dịch có giá trị pH lớn nhất là
A
KNO₃
B
H₂SO₄
C
Na₂CO₃
D
HCl
Câu 4Thông hiểu
Xem chi tiết →Trong các phản ứng hữu cơ thường có sự tạo thành các tiểu phân trung gian hoạt động như gốc tự do, carbanion, carbocation. Carbocation là ion mang điện tích dương trên nguyên tử carbon. Có bao nhiêu carbocation trong số các tiểu phân sau:
\((CH_3)_3C^+\),
\((CH_3)_2CH^-\),
\(CH_3^\bullet\),
\(CH_3CH_2^\bullet\),
\(CH_3-C\equiv C^-\)?
\((CH_3)_3C^+\),
\((CH_3)_2CH^-\),
\(CH_3^\bullet\),
\(CH_3CH_2^\bullet\),
\(CH_3-C\equiv C^-\)?
A
1
B
2
C
4
D
3
Câu 5Nhận biết
Xem chi tiết →Cho bảng giá trị thế điện cực chuẩn của các cặp oxi hóa – khử như sau:
| Cặp oxi hóa – khử | E⁰ (V) |
|--------------------|--------|
| Al³⁺/Al | -1,676 |
| Fe²⁺/Fe | -0,440 |
| Cu²⁺/Cu | +0,340 |
| Ag⁺/Ag | +0,799 |
Dựa vào bảng thế điện cực chuẩn trên, kim loại có tính khử mạnh nhất là
| Cặp oxi hóa – khử | E⁰ (V) |
|--------------------|--------|
| Al³⁺/Al | -1,676 |
| Fe²⁺/Fe | -0,440 |
| Cu²⁺/Cu | +0,340 |
| Ag⁺/Ag | +0,799 |
Dựa vào bảng thế điện cực chuẩn trên, kim loại có tính khử mạnh nhất là
A
Fe
B
Ag
C
Cu
D
Al
Câu 6Nhận biết
Xem chi tiết →Chất nào sau đây thuộc loại polysaccharide?
A
Fructose.
B
Saccharose.
C
Cellulose.
D
Glucose.
Câu 7Thông hiểu
Xem chi tiết →Catechin là một chất kháng oxi hoá mạnh, ức chế hoạt động của các gốc tự do nên có khả năng phòng chống bệnh ung thư, nhồi máu cơ tim. Công thức cấu tạo của catechin được cho như hình dưới:
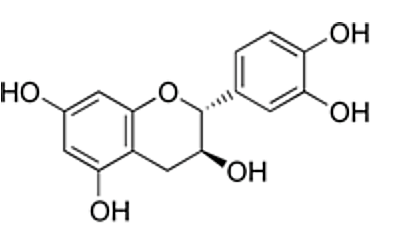
Phát biểu nào sau đây không đúng?

Phát biểu nào sau đây không đúng?
A
Phân tử catechin có 4 nhóm -OH phenol.
B
Catechin có phân tử khối là 290.
C
Công thức phân tử của catechin là \( \ce{C15H16O6} \).
D
Catechin phản ứng được với dung dịch NaOH.
Câu 8Nhận biết
Xem chi tiết →Ở trạng thái cơ bản, số electron ở lớp ngoài cùng trong nguyên tử Al (Z=13) là
A
3
B
2
C
1
D
4
Câu 9Thông hiểu
Xem chi tiết →Phương pháp điện phân nóng chảy được sử dụng để điều chế kim loại nào sau đây?
A
Al
B
Fe
C
Ag
D
Cu
Câu 10Thông hiểu
Xem chi tiết →Xăng E5 chứa 5% thể tích ethanol hiện đang được sử dụng phổ biến ở nước ta để thay thế một phần xăng thông thường. Một người đi xe máy mua 3 lít xăng E5 để đổ vào bình chứa nhiên liệu. Thể tích ethanol có trong 3 lít xăng trên là
A
75 mL.
B
125 mL.
C
100 mL.
D
150 mL.
Hiển thị 10 trên 20 câu hỏi